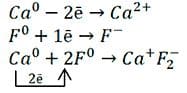ГЛАВА V. Химическая связь. Окислительно-восстановительные реакции
§34. Ионная химическая связь
Вопрос в начале параграфа
✓ Атомы элементов−металлов легко отдают электроны с внешнего энергетического уровня, превращаясь при этом в положительные ионы. Атомы элементов−неметаллов принимают недостающие электроны до завершения внешнего энергетического уровня, превращаясь при этом в отрицательные ионы. Каков же дальнейший химический результат таких процессов?
Ответ:
Рассмотрим, как это происходит при взаимодействии атомов натрия и хлора. Атом натрия, как элемент IA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свой единственный электрон с внешнего уровня атому хлора. Атому хлора, как элементу VIIA−группы, как раз и не хватает одного электрона для завершения внешнего слоя. При этом атом натрия превратится в положительно заряженный ион с зарядом 1+, а атом хлора — в отрицательно заряженный ион с зарядом 1–. Напомним, что ионы — это положительно или отрицательно заряженные частицы, в которые превращаются атомы химических элементов в результате отдачи или присоединения электронов. Между разноимённо заряженными ионами возникнет электростатическое притяжение. Образуется хорошо знакомое всем соединение — хлорид натрия (поваренная соль):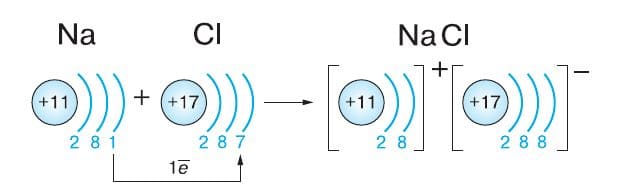
Химическую связь, образующуюся между ионами за счёт электростатического притяжения, называют ионной связью.
Проверьте свои знания
1. Что такое ионы? Как они образуются?
Ответ:
Ионы — это положительно или отрицательно заряженные частицы, в которые превращаются атомы химических элементов в результате отдачи или присоединения электронов.
Ионы образуются в результате отдачи или присоединения электронов атомами.
2. Найдите сходство и различия между: а) атомом кальция и ионом кальция; б) атомом кислорода и ионом кислорода.
Ответ:
а) Сходство и различия между атомом кальция и ионом кальция:
Сходства: заряд ядра +20; относительная атомная масса 40.
Различия: атом электронейтрален, а ион имеет заряд +2; атом имеет 2 внешних электрона, а ион − 8 внешних электронов.
б) Сходство и различия между атомом кислорода и ионом кислорода:
Сходства: заряд ядра +8; относительная атомная масса 16.
Различия: атом электронейтрален, а ион имеет заряд −2; атом имеет 6 внешних электронов, а ион 8 внешних электронов.
Примените свои знания
3. Составьте схему образования ионной связи между литием и элементами−неметаллами: а) фтором; б) кислородом; в) азотом.
Ответ:
а) Схема образования ионной связи между литием и фтором:
Атом лития, как элемент IA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свой единственный электрон с внешнего уровня атому фтора. Атому фтору, как элементу VIIА−группы, как раз и не хватает одного электрона для завершения внешнего слоя. При этом атом лития превратится в положительно заряженный ион с зарядом 1+, а атом фтора — в отрицательно заряженный ион с зарядом 1–.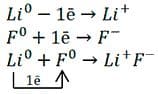
б) Схема образования ионной связи между литием и кислородом:
Атом лития, как элемент IA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свой единственный электрон с внешнего уровня атому кислорода. Атому кислорода, как элементу VIA−группы, не хватает двух электронов для завершения внешнего слоя. При этом атом лития превратится в положительно заряженный ион с зарядом 1+, а атом кислорода − в отрицательно заряженный ион с зарядом 2–.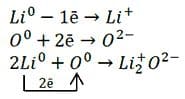
в) Схема образования ионной связи между литием и азотом:
Атом лития, как элемент IA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свой единственный электрон с внешнего уровня атому азота. Атому азота, как элементу VA−группы, не хватает трех электронов для завершения внешнего слоя. При этом атом лития превратится в положительно заряженный ион с зарядом 1+, а атом азота − в отрицательно заряженный ион с зарядом 3–.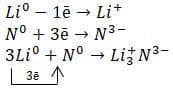
4. Составьте схему образования ионной связи между фтором и элементами−металлами: а) калием; б) кальцием; в) алюминием.
Ответ:
а) Схема образования ионной связи между фтором и калием:
Атом калия, как элемент IA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свой единственный электрон с внешнего уровня атому алюминия. Атому фтора, как элементу VIIA−группы, как раз и не хватает одного электрона для завершения внешнего слоя. При этом атом калия превратится в положительно заряженный ион с зарядом 1+, а атом фтора − в отрицательно заряженный ион с зарядом 1–.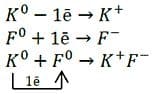
б) Схема образования ионной связи между фтором и кальцием:
Атом кальция, как элемент IIA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свои два электрона с внешнего уровня атому фтора. Атому фтору, как элементу VIIA−группы, не хватает одного электрона для завершения внешнего слоя. При этом атом кальция превратится в положительно заряженный ион с зарядом 2+, а атом фтора − в отрицательно заряженный ион с зарядом 1–.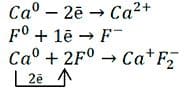
в) Схема образования ионной связи между фтором и алюминием:
Атом алюминия, как элемент IIIA−группы периодической системы Д. И. Менделеева, для получения завершённого внешнего энергетического уровня отдаст свои три электрона с внешнего уровня атому фтора. Атому фтору, как элементу VIIA−группы, не хватает одного электрона для завершения внешнего слоя. При этом атом алюминия превратится в положительно заряженный ион с зарядом 3+, а атом фтора − в отрицательно заряженный ион с зарядом 1–.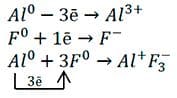
5. Найдите соотношение чисел положительных и отрицательных ионов в соединениях: а) хлорид натрия NaCl; б) хлорид кальция $CaCl_{2}$; в) фторид алюминия $AlF_{3}$.
Ответ:
а) Хлорид натрия: NaCl = $Na^{+}$ + $Cl^{-}$
Таким образом, соотношение чисел положительных и отрицательных ионов 1 : 1.
б) Хлорид кальция: $CaCl_{2}$ = $Ca^{2+}$ + 2$Cl^{-}$
Таким образом, соотношение чисел положительных и отрицательных ионов 1 : 2.
в) Фторид алюминия: $AlF_{3}$ = $Al^{3+}$ + 3$F^{-}$
Таким образом, соотношение чисел положительных и отрицательных ионов 1 : 3.
Используйте дополнительную информацию
6. Предложите свой вариант графического отображения образования химической связи в соединении, имеющем формулу $CaF_{2}$.
Ответ:
Атом кальция, как элемент IIA−группы периодической системы Д. И. Менделеева, для превращения завершённого предвнешнего энергетического уровня во внешний отдаст два электрона с внешнего уровня.
Атому фтора, как элементу VIIA−группы, не хватает одного электрона для завершения внешнего слоя. При этом атом кальция превратится в положительно заряженный ион с зарядом 2+, а атом фтора − в отрицательно заряженный ион с зарядом 1–.