Ответы к §2. Предмет химии. Вещества
Лабораторный опыт №1
Сравнение свойств твёрдых кристаллических веществ и растворов.
Сравните, используя приведённый на с. 10 план, свойства выданных вам в стаканчиках образцов веществ:
вариант 1 − кристаллических сахара и поваренной соли;
вариант 2 − глюкозы и лимонной кислоты.
Ответ:
Вариант 1.
Свойства Кристаллический сахар Поваренная соль
Агрегатное
состояние Твёрдое Твёрдое
Цвет Бесцветное Бесцветное
Запах Без запаха Без запаха
Твёрдость
по шкале Мосса 2 2
Физические
свойства Не пластичен Не пластичен
и не эластичен и не эластичен
Растворимость Растворим Растворим
в воде в воде
Температура 186°C 801°C
плавления
Температура
кипения -* 1465 °C
Плотность 1,587 $г/см^3$ 2,165 $г/см^3$
Тепло- и В сухом виде В сухом виде
электро- не проводит не проводит
проводность эл. ток и тепло эл. ток и тепло.
В виде раствора или расплава
обладает тепло − и электропроводностью
*при более высокой температуре сахар карамелизуется, поэтому температуры кипения не имеет.
Вариант 2.
Свойства Глюкоза Лимонная кислота
Агрегатное
состояние Твёрдое Твёрдое
Цвет Белый Белый цвет,
имеет блеск
Запах Без запаха Без запаха
Твёрдость по
шкале Мосса 2 2
Физические
свойства Не пластичен Не пластичен
и не эластичен и не эластичен
Растворимость Растворима Растворима
в воде в воде
Температура 146°C 153 °C
плавления
Температура
кипения -* -*
Плотность 1,56 $г/см^3$ 1,66 $г/см^3$
Тепло- и
электро-
проводность Не проводит Не проводит
эл. ток и тепло эл. ток и тепло.
*при плавлении разлагается, поэтому температуры кипения нет.
i. Работа в информационной среде
1. Найдите в Интернете электронные адреса, раскрывающие содержание ключевых слов и словосочетаний параграфа для создания классного банка данных.
Ответ:
1.http://www.hemi.nsu.ru/ucheb113.htm
2.https://himi4ka.ru/arhiv−urokov/urok−1−atomy−i−himicheskie−jelementy.html
3.https://himi4ka.ru/arhiv−urokov/urok−3−molekuly−i−prostye−veshhestva.html
4. https://ru.wikipedia.org/wiki/Вещество%28химия%29#:~:text=Вещества%20в%20химии%20принято%20разделять,железо,%20озон,%20алмаз,%20азот,%20…%29
5.https://ru.wikipedia.org/wiki/Химическийэлемент
2. Используя ресурсы Интернета, подготовьте информационный продукт (по выбору): презентацию по теме урока или сообщение по одному из ключевых слов (словосочетаний) параграфа.
Ответ:
Вещества простые и сложные
Простым называют вещество, состоящее из однотипных атомов, то есть образованное одним элементом. Его нельзя разложить на другие вещества.
Простые вещества подразделяют на две группы:
−металлы: натрий, алюминий, марганец, золото, железо и т. д.;
−неметаллы: кислород, озон, водород, хлор, графит и пр.
Если атомы связаны в молекулы, то простое вещество считается соединением (бром, фосфор, большинство газов). В отличие от них, металлы, алмаз, графит, инертные газы – это атомарные вещества.
Понятие простого вещества необходимо отличать от понятия химического элемента. Элемент – это совокупность химически одинаковых атомов. В свободном виде он существует в форме природного или искусственного простого вещества.
Характеристики химического элемента:
− атомный номер;
− относительная атомная масса;
− распространенность;
− изотопный состав;
− валентность;
− химический символ.
Примеры высказываний:
− относительная атомная масса хлора равна 35,5;
− азот входит в состав многих соединений.
Характеристики простых веществ:
− физические свойства (магнитные, оптические, термические и пр.);
− молярная масса;
− растворимость;
− токсичность;
− химическая формула.
Примеры высказываний:
− молекула хлора имеет относительную массу 71;
− азот входит в состав атмосферы.
Сложное вещество построено из химически связанных атомов различных элементов. Получение и разложение сложных веществ осуществляется в химических реакциях. Это отличает их от смесей.
Классификация сложных химических веществ.
Исходя из строения и свойств, выделяют следующие классы сложных соединений:
1. бинарные. Это вещества, образованные двумя элементами: гидриды (CaH2, KH), карбиды (SiC, Mg2C) бескислородные кислоты (соляная HCl, сероводород H2S) и их соли (хлориды, сульфиды и др.).
2. оксиды. Это сложные бинарные вещества, в составе которых есть кислород со степенью окисления (условным зарядом иона) −2. Различают основные K2O, MgO (степень окисления металла +1, +2), кислотные SO3, CO2, CrO3 с неметаллами или металлами в степени окисления от +5 до +7, амфотерные ZnO, Al2O3 и несолеобразующие (CO, SiO, NO и N2O) оксиды.
3. гидроксиды характеризуются составом вида «элемент – группа OH». К этому классу веществ относят:
− кислоты (азотная HNO3, фосфорная H3PO4, серная H2SO4). Образуются в результате взаимодействия кислотных оксидов с водой. Имеют в составе один или несколько атомов водорода, которые могут замещаться атомом металла, и кислотный остаток.
− основания (едкий натр NaOH, гашеная известь Ca(OH)2), образующиеся в реакциях воды с основными оксидами. Растворимые основания (KOH, NaOH) называются щелочами.
− амфотерные гидроксиды способны проявлять и кислотные, и основные свойства.
4. Соли. Это сложные химические вещества с составом типа «металл – кислотный остаток». Соль – продукт реакции между кислотой и основанием. Карбонат калия (поташ) K2(CO)3, сульфат меди (медный купорос) CuSO4 – примеры солей.
?. Вопросы и задания
1. Филео (греч.) означает «люблю», фобос − «боюсь». Дайте объяснение терминов «хемофилия» и «хемофобия», отражающих резко противоположное отношение групп людей к химии. Кто из них прав? Обоснуйте свою точку зрения.
Ответ ©:
Хемофилия — «любовь к химии», хемофобия — «боязнь химии». Это две крайности отношения к химии, поэтому моя точка зрения лежит где-то посередине. С одной стороны, без химии невозможна жизнь современного человека, поскольку любое промышленное производство - это химия. Человек научился изготавливать пластмассы из нефти, извлекать металлы из руд, делать лекарства, удобрения, инсектициды. Без всего этого современная жизнь немыслима. С другой стороны, многие продукты и выбросы химической промышленности загрязняют окружающую среду, все больше химических веществ применяется в производстве продуктов питания, а это вредно для здоровья человека.
2. Обязательный атрибут множества детективных произведений — цианистый калий, точнее, цианид калия, который обладает свойством парализовывать нервную систему, приводя тем самым жертву к мгновенной смерти. Приведите примеры свойств других веществ, которые используются в литературных произведениях.
Ответ:
Свойство белого фосфора светиться при окислении кислородом воздуха использовано в детективе Артура Конана Дойла "Собака Баскервилей" , собака светилась из−за того, что она была обмазана белым фосфором с каким−то другим веществом без запаха.
В повести Михаила Афанасьевича Булгакова "Собачье сердце" используется хлороформ в качестве наркоза во время хирургической операции.
В романе Жюль Верна "Таинственный остров" описывается способ получения нитроглицерина, который они использовали для того, чтобы взорвать гранитную скалу. Нитроглицерин в те времена широко применялся во взрывотехнике. В чистом виде он очень неустойчив и взрывоопасен.
В романе Александра Дюма "Граф Монте−Кристо" граф Монте−Кристо рассказывает популярный способ убийства с помощью мышьяка, который продавался в аптеках того времени. Мышьяк и все его соединения ядовиты.
В романе Алексея Николаевича Толстого "Гиперболоид инженера Гарина" описан способ получения тетрила, обладающий большой силой взрыва.
В рассказе писателя Николая Носова "Бенгальские огни" рассказывалось о том, как самому сделать бенгальские огни, в рецепте говорилось о ряде веществ: сера, сахар, алюминиевые опилки.
В произведении Владимира Короткевича "Черный замок Ольшанский. Дикая охота короля Стаха" есть эпизод, про пещеру в которую человек войдет и ходит, а собака или кролик погибают через несколько минут. Речь идет об углекислом газе, который собирается внизу пещеры: человеческая голова выше этой зоны, а собачья и кроличья – нет.
В фантастическом романе Александра Богданова "Красная звезда" приведено описание космического корабля, в котором хранились запасы кислорода в виде 25 тонн бертолетовой соли, из которой можно было выделить кислород. При нагревании хлората калия выделяется кислород.
В романе Генри Райдер Хаггарда "Клеопатра" есть следующие строки: "…она вынула из уха одну из тех огромных жемчужин… и… опустила жемчужину в уксус. Наступило молчание, потрясенные гости, замерев, наблюдали, как несравненная жемчужина медленно растворяется в крепком уксусе. Вот от нее не осталось и следа…". Карбонат кальция, из которого состоит жемчужина, реагирует с уксусной кислотой, эта реакция описывается в произведении.
3. Выпишите отдельно названия веществ и названия тел из приведённого перечня: медь, монета, стекло, стакан, ваза, керамика, проволока, алюминий. Воспользуйтесь подсказкой: к названию тела − существительному – можно подобрать относительное прилагательное, образованное от названия вещества, например: железо и гвоздь − железный гвоздь.
Ответ:
Вещество Тело
Медь Монета
Стекло Стакан
Керамика Ваза
Алюминий Проволока
4. Выпишите качественные прилагательные: лёгкий, круглый, длинный, тяжёлый, твёрдый, пахучий, растворимый, увесистый, вогнутый, мягкий, жидкий, прозрачный, − которые могут быть отнесены:
а) к веществам; б) к телам; в) и к телам, и к веществам.
Ответ:
Вещества Тела Вещества и тела
Пахучий Круглый Лёгкий
Растворимый Длинный Тяжёлый
Жидкий Увесистый Твёрдый
Прозрачный Вогнутый Мягкий
5. Сравните понятия «простое вещество» и «сложное вещество». Найдите сходство и различие.
Ответ:
Сходство состоит в том, что любые вещества состоят из атомов. Но простые вещества образованы атомами одного химического элемента, а сложные вещества образованы атомами разных химических элементов.
6. Определите, какие из веществ, модели молекул которых изображены на рисунке 2 на с.5, относят:
а) к простым веществам; б) к сложным веществам.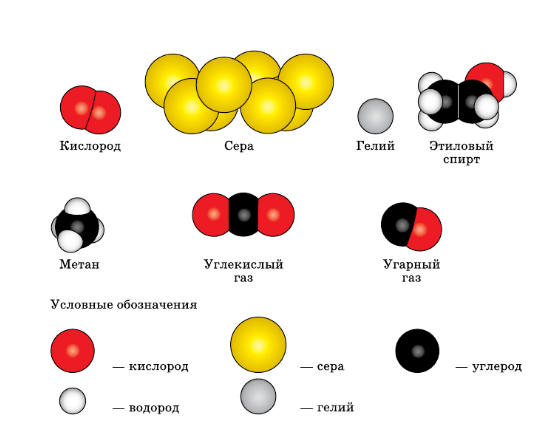
рис. 2. Модели молекул некоторых веществ
Ответ:
Простые вещества: кислород (O2), сера (S), гелий (He).
Сложные вещества: этиловый спирт (C2H5OH), метан (CH4), углекислый газ (CO2), угарный газ (CO).
7. Какое понятие более широкое — «химический элемент» или «простое вещество»? Дайте доказательный ответ.
Ответ ©:
Понятие "химический элемент" более широкое по сравнению с понятием "простое вещество". Один химический элемент может образовывать различные вещества - и простые, и сложные. Например, химический элемент водород может образовать простое вещество водород (Н2) и множество сложных веществ (неорганические кислоты, основания, органические и другие вещества)
8. Укажите, где о кислороде говорится как о химическом элементе, а где − как о простом веществе:
а) кислород мало растворим в воде;
б) молекулы воды состоят из двух атомов водорода и одного атома кислорода;
в) в воздухе содержится 21% кислорода (по объёму);
г) кислород входит в состав углекислого газа.
Ответ:
Кислород как химический элемент: б), г).
Кислород O как химический элемент представлен атомами в составе воды H2O, углекислого газа СO2.
Кислород как простое вещество: а), в).
Кислород O2 как простое вещество − газ, плохо растворимый в воде, имеет объёмную долю 21% в атмосферном воздухе.
9. Укажите, где о водороде говорится как о простом веществе, а где − как о химическом элементе:
а) водород входит в состав большинства органических соединений;
б) водород − самый лёгкий газ;
в) водородом заполняют воздушные шары;
г) молекула метана содержит четыре атома водорода.
Ответ:
Водород как химический элемент: а), г).
Водород Н как химический элемент представлен атомами в составе молекул метана (CН4) и других органический соединений.
Водород как простое вещество: б), в).
Водород Н2 как простое вещество − газ.
10. Рассмотрите связь между свойствами вещества и его применением на примере:
а) стекла;
б) полиэтилена;
в) сахара;
г) железа.
Ответ:
а) Свойства стекла:
− Прозрачность, поэтому его применяют для изготовления оптических приборов, оконных стекол, изготовления посуды, в том числе лабораторной, оптического волокна.
− Низкая теплопроводность, поэтому его применяют для изготовления утеплителей (пеностекло, стекловата).
− Химическая инертность, поэтому его применяют для изготовления лабораторной посуды и оборудования, остекловывания радиоактивных отходов.
б) Свойства полиэтилена:
− Прозрачность и эластичность, поэтому его применяют для производства плёнки, упаковки.
− Амортизационность, поэтому его применяют для изготовления тары (бутылки, канистры и т. д.), бронежилетов.
− Химическая инертность в отношении щелочей и солей, поэтому его применяют для изготовления упаковки щелочесодержащих продуктов.
в) Сахар растворим в воде, имеет сладкий вкус, съедобен, поэтому его применяют в пищевой промышленности.
г) Свойства железа:
− Распространенность в земной коре, дешевизна, ковкость, металлический блеск. Из−за совокупности этих свойств железо является основным компонентом сталей и чугунов.
− Ферромагнитные свойства, поэтому его применяют в электротехнике для изготовления магнитопроводов, трансформаторов и электродвигателей.

