Глава 3. Вещества вокруг нас
§17 Воздух и кислород
Вопросы перед параграфом
Задание №1
Из чего состоит воздух?
Ответ
Воздух − это смесь газов.
В его состав входят:
1. Азот ($N_{2}$)
2. Кислород ($O_{2}$)
3. Инертный газ Аргон (Ar)
4. Углекислый газ ($CO_{2}$)
5. Инертный газ Неон (Ne)
6. Инертный газ Гелий (He)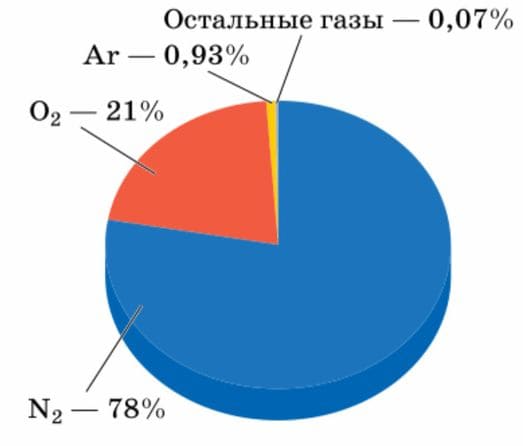
Рис.81. Состав сухого воздуха
Задание №2
Как разделить воздух на отдельные вещества?
Ответ
Для разделения воздуха на отдельные вещества его сначала сжижают путём повышения давления и понижения температуры. Затем, полученную жидкость разделяют на отдельные газы (фракции) при помощи фракционной перегонки.
Температура кипения жидкого кислорода −182,98 °C.
Температура кипения жидкого аргона −185,9°C.
Температура кипения жидкого азота −195,8°C.
Эта разность температур кипения и позволяет разделить смесь.
Задание №3
Чем воздух по свойствам отличается от чистого кислорода?
Ответ
1. Чистым кислородом нельзя дышать в течение долгого времени.
2. Воздух − это смесь газов, кислород − это чистое вещество.
3. При чистом кислороде реакция горения будет происходить более бурно.
4. Чистый кислород окисляет вещества быстрее, чем воздух.
Задание №4
Как в атмосфере появился кислород?
Ответ
Кислород начал появляться в атмосфере в результате фотосинтеза, осуществляемого в Мировом океане бактериями и синезелёными водорослями. Поглощая солнечный свет, они превращали углекислый газ в органические вещества. В качестве побочного продукта этой реакции образовывался молекулярный кислород, который из−за плохой растворимости в воде выделялся в атмосферу.
(стр.109)
Задание №1
Раздел «Занимательные опыты».
Подробнее познакомиться с получением одного из оксидов нам поможет опыт 2 (с.178).
Ответ
Опыт 2. Горение магния
Возьмите пинцетом кусок магниевой стружки так, чтобы основная часть стружки торчала наружу. Опыт проводите на чистом столе над металлическим противнем с песком. Рядом с противнем на столе поместите подставку под горючее, на неё положите одну таблетку сухого топлива и подожгите её спичкой. Внесите в верхнюю часть пламени магниевую ленту. Как только она загорится, расположите руку с держателем над противнем. Когда лента сгорит и держатель остынет, рассмотрите белый порошок, образовавшийся при горении магния. Это жжёная магнезия — оксид магния MgO. Её добавляют в состав не которых кремов и мазей. Опыт эффектно наблюдать в темноте. Попробуйте провести его вечером на открытом воздухе.
(стр.111)
Задание №1
Раздел «Занимательные опыты».
Для получения кислорода и изучения его свойств выполните опыт 5 (с.179−180).
Ответ
Опыт 5. Получаем кислород
Познакомимся со свойствами ещё одного неметалла — кислорода. Кислород входит в состав воздуха — в нём его 21% по объёму. Мы получим чистый кислород. Для этого используем перекись водорода. Это вещество способно разлагаться на воду и кислород. Перекись водорода при хранении разлагается постепенно, поэтому хранят её в темноте. Аптечная 3%−я перекись поступает в продажу в склянках из коричневого стекла. Для ускорения разложения перекиси используем оксид марганца. В химический стакан налейте примерно 5 мл перекиси. На кончике шпателя внесём в стакан с перекисью оксид марганца. Перекись вспенивается. Это выделяется кислород. Убедиться, что выделившийся газ — кислород, можно с помощью тлеющей лучинки. Для этого зажгите лучинку и, когда она разгорится, потушите её, но не полностью, а так, чтобы на её конце остался тлеющий уголёк. Внесите тлеющую лучинку в стакан с перекисью, опустив её как можно ниже, но не касаясь раствора (иначе лучинка погаснет). Лучинка вспыхнет. Это свидетельствует о том, что при разложении перекиси выделяется кислород.
(стр.113)
Задание №1
В определённые периоды истории Земли концентрация кислорода в воздухе превышала ныне существующую. Такая атмосфера была химически очень активной, поэтому на Земле часто происходили лесные пожары. Определите по графику (см. рис. 84), сколько миллионов лет назад содержание кислорода в атмосфере превышало 30%.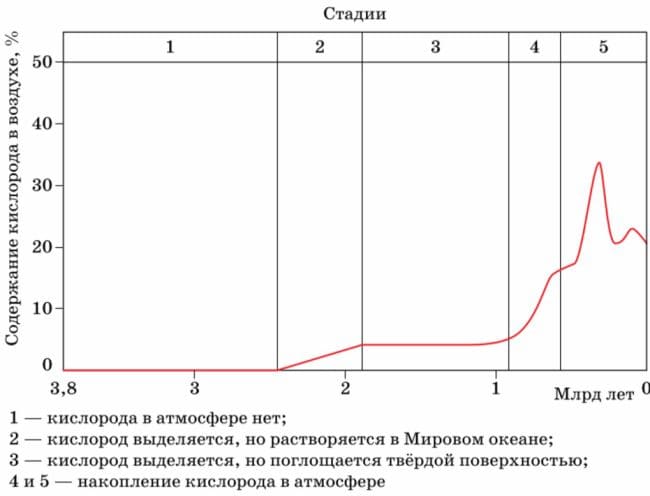
Рис. 84. Изменение содержания кислорода в атмосфере за время существования Земли
Ответ
Содержание кислорода в атмосфере превышало 30% примерно 300 миллионов лет назад.
§17. проблемный вопрос
Задание №1
Есть ли атмосфера у Солнца? А у других планет Солнечной системы?
Ответ
У Солнца есть атмосфера, которую принято разделять на фотосферу, хромосферу и корону. Также у всех планет Солнечной системы есть атмосфера, кроме Меркурия.
§17. вопросы и задания
Задание №1
Плотность воды равна 1 кг/л. Во сколько раз воздух легче воды?
Ответ
Дано:
p ($H_{2}O$) = 1 кг/л = 1000 г/л
p(воздуха) = 1,29 г/л
Найти:
$\frac{p(H_{2}O)}{p(воздуха)}$ − ?
Решение:
$\frac{p(H_{2}O)}{p(воздуха)}$ = $\frac{1000}{1,29}$ = 775 раз
Ответ: Плотность воды в 775 раз больше плотности воздуха.
Задание №2
Чему равна объёмная доля кислорода в воздухе?
Ответ
Объёмная доля кислорода в воздухе равна 21%.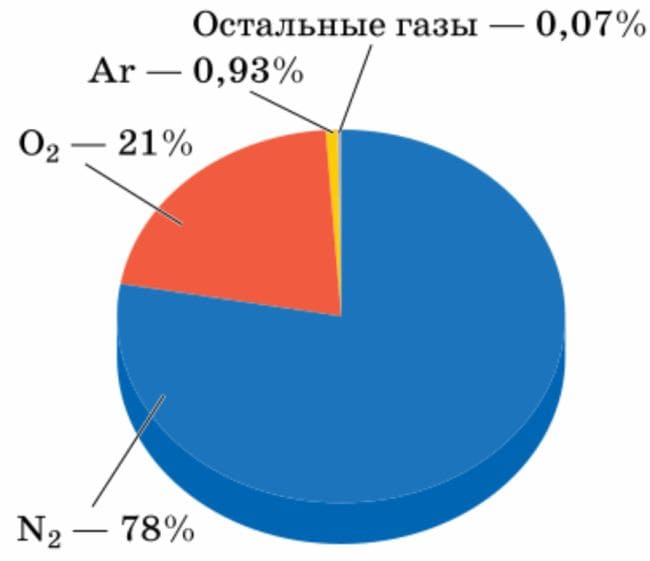
Рис.81. Состав сухого воздуха
Задание №3
Сколько миллилитров углекислого газа содержится в одном кубометре воздуха?
Ответ
Дано:
V(возд.) = $1м^3$ = $10^6$ мл
w ($CO_{2}$) = 0,04%
Найти:
V($CO_{2}$) − ?
Решение:
V($CO_{2}$) = $\frac{w(CO_{2})*V(возд.)}{100}$ = $\frac{0,04 * 106 мл}{100}$ = 400 мл
Ответ: V ($CO_{2}$) = 400 мл
Задание №4
Составьте уравнение окисления глюкозы в организме.
Ответ
Окисление глюкозы − это взаимодействие глюкозы и кислорода. В ходе реакции выделяется углекислый газ и вода.
$C_{6}H_{12}O_{6}$ + 6$O_{2}$ = 6$CO_{2}$ + 6$H_{2}O$
Задание №5
Взаимодействуя с аммиаком, кислород превращает его в азот и воду. Составьте уравнение этой реакции.
Ответ
Формула аммиака: $NH_{3}$.
4$NH_{3}$+3$O_{2}$ = 2$N_{2}$+6$H_{2}O$
Задание №6
Различия в каком свойстве позволяют разделить воздух на азот и кислород?
Ответ
Разделение основано на различии температур кипения сжиженного азота (–196°С) и кислорода (–183°С). Если сжижать воздух, а затем дать ему испариться, то в газообразную фазу будет переходить более низкокипящий компонент (азот), и пары обогатятся им, а жидкость – кислородом.
Задание №7
В каких областях промышленности применяют кислород?
Ответ
Кислород применяют в ракетостроении (в качестве топлива), в медицине, в металлургии, при сварке.
Задание №8
При разложении перекиси водорода $H_{2}O_{2}$ образуются кислород $O_{2}$ и вода $H_{2}O$. Составьте уравнение этой реакции.
Ответ
2$H_{2}O_{2}$ = $O_{2}$+2$H_{2}O$
Задание №9
Какие газы являются наиболее токсичными для организма? Откуда они берутся в атмосфере?
Ответ
Для организма наиболее токсичными газами являются сероводород ($H_{2}S$), сернистый газ $SO_{2}$ и хлор ($Cl_{2}$), которые попадают в воздух в результате деятельности химических, нефтехимических и металлургических производств. Очень ядовитым газом также является озон ($O_{3}$), который может образовываться из кислорода в загрязнённой атмосфере мегаполисов в яркий солнечный день.
(стр.114)
Задание №1
В XVIII в. были открыты и изучены многие газообразные вещества. Их часто называли «воздухом», добавляя прилагательное, характеризующее новый газ. Используя информационные ресурсы, объясните, что такое «горючий воздух», «огненный воздух», «связанный воздух», «морской кислотный воздух», «щелочной воздух».
Ответ
Горючий воздух − это первое название водорода ($H_{2}$).
Огненный воздух − это первое название кислорода ($O_{2}$).
Связанный воздух − это первое название углекислого газа ($CO_{2}$).
Морской кислотный воздух − это первое название хлористого водорода ($HCl$).
Щелочной воздух − это первое название аммиака ($NH_{3}$).

