§4 Как устроен атом
Вопросы перед параграфом
Задание №1
Какие частицы считаются элементарными?
Ответ
Элементарные частицы − собирательный термин, относящийся к микрообъектам, которые на данный момент на практике невозможно расщепить на составные части.
Задание №2
Какие элементарные частицы входят в состав атомов?
Ответ
Во всех атомах есть три типа элементарных частиц:
1) электроны (e) − имеют отрицательный заряд, равный –1
2) протоны (p) − имеют положительны заряд, равный +1
3) нейтроны (n) − заряда не имеют, это электронейтральные частицы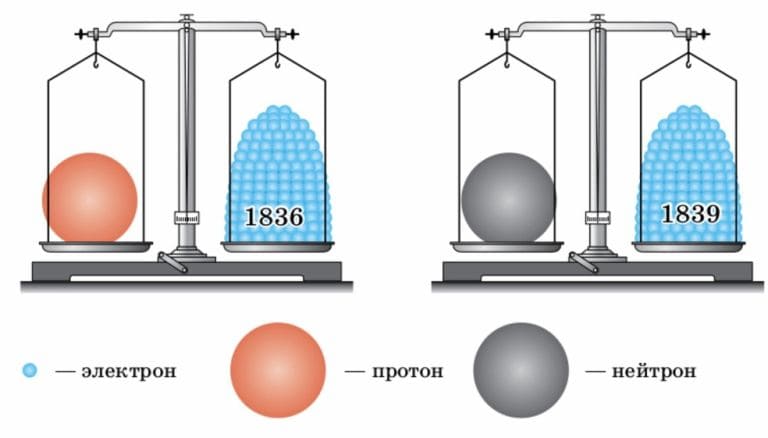
Рис. 20 Строение атома углерода
Массы протона и нейтрона почти одинаковы и намного, почти в 2000 раз, превышают массу электрона.
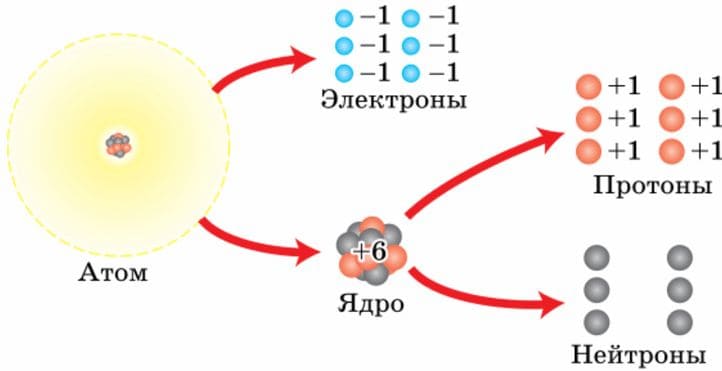
Рис. 21 Условное изображение строения атомов
Проблемный вопрос
Задание №1
Как доказать, что атом − не элементарная частица, а в атоме есть ядро.
Ответ
Доказать, что атом − не элементарная частица, помогли физики. Открытие радиоактивности и существования неустойчивых атомов подтвердило идею о сложном строении атома: если некоторые атомы распадаются, то они уже не могут считаться элементарными частицами. Значит, атом состоит из более простых частиц.
Мы знаем, что во всех атомах есть три типа элементарных частиц: электроны (e), протоны (p) и нейтроны (n). Каждая частица характеризуется электрическим зарядом и массой.
Протоны и нейтроны образуют ядро, которое находится в центре атома.
Вопросы и задания
Задание №1
Если представить атом размером с Луну (диаметр 3500 км), то каким будет радиус его ядра.
Ответ
Дано:
D (атома) = 3500 км = 3500000 м
Найти:
R (ядра) − ?
Решение:
Т.к. ядро атома примерно в 100 тыс. раз меньше размера атома, то есть $\frac{D (атома)}{D (ядра)}$ = 100000, следовательно,
D (ядра) = $\frac{D (атома)}{100000}$ = $\frac{3500000 м}{100000}$ = 35 м
R (ядра) = $\frac{D (ядра)}{2}$ = $\frac{35 м}{2}$ = 17,5 м
Ответ: R (ядра) = 17,5 м
Задание №2
Если бы ядро атома имело радиус, равный толщине волоса (0,08 мм), то каким был размер атома?
Ответ
Дано:
R (ядра) = 0,08 мм
Найти:
D (атома) − ?
Решение:
Т.к. ядро атома примерно в 100 тыс. раз меньше размера атома, то есть $\frac{D(атома)}{D (ядра)}$ = 100000, следовательно,
D (ядра) = R (ядра) * 2 = 0,16 мм
D (атома)= D (ядра) * 2 = 0,16 * 100000 = 16000 мм = 16 м
Ответ: D (атома) = 16 м
Задание №3
Чему равно массовое число самого лёгкого атома?
Ответ
Самый лёгкий атом у водорода (H), его массовое число равно 1.
Задание №4
Назовите атом, строение которого изображено на рисунке 23, определите его массовое число, заряд ядра и число нейтронов.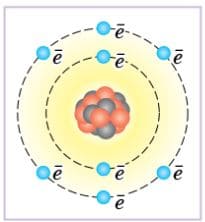 Рис.23. Условное изображение строения атома
Рис.23. Условное изображение строения атома
Ответ
1) Количество электронов равно 8, а число электронов = порядковому номеру элемента, значит это элемент с порядковым №8, т.е. это кислород (O).
2) Массовое число A = 16.
3) Заряд ядра +8.
4) Число нейтронов:
A (массовое число) − Z (количество протонов) = 16 − 8 = 8 нейтронов.
Задание №5
Назовите элементы, атомы которых содержат:
а) 2 ē;
б) 10 ē;
в) 18 ē;
г) 36 ē;
д) 54 ē;
е) 86 ē.
Ответ
а) 2 ē − Гелий (порядковый №2)
б) 10 ē − Неон (порядковый №10)
в) 18 ē − Аргон (порядковый №18)
г) 36 ē − Криптон (порядковый №36)
д) 54 ē − Ксенон (порядковый №54)
е) 86 ē − Радон (порядковый №86)
Число электронов = число протонов = порядковый номер элемента.

