§25. Кислоты, их классификация и химические свойства. Часть I
Задание №1
Кислоты − это _
Ответ:
Кислоты — это сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка.
Задание №2
Оформите схему "Классификация кислот".
Ответ:
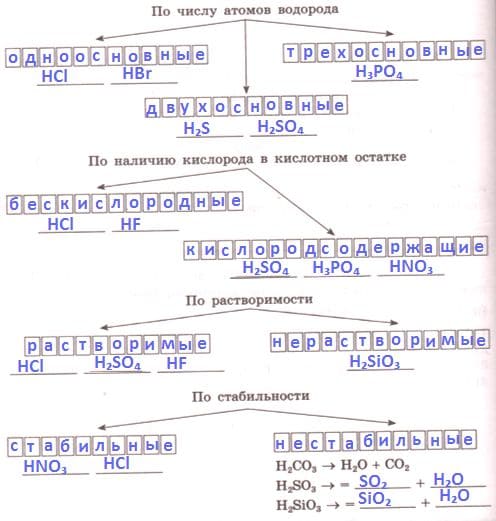
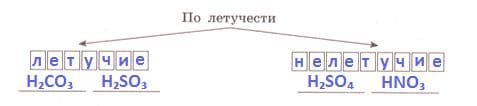
Задание №3
Кислоты взаимодействуют:
1) с металлами, расположенными в ряду активности до водорода
Zn + HCl = _ + _
2) с оксидами металлов
$CuO + H_{2}SO_{4}$ = _ + _
$Fe_{2}O_{3} + HNO_{3}$ = _ + _
3) с гидроксидами металлов
$Ca(OH)_ {2} + H_{3}PO_{4}$ = _ + _
$Al(OH)_ {3} + HCl$ = _ + _
4) с солями, если образуется ↑ или ↓
$CaCO_{3} + HNO_{3}$ = _ + _
$BaCl_{2} + H_{2}SO_{4}$ = _ + _
Ответ:
Кислоты взаимодействуют:
1) с металлами, расположенными в ряду активности до водорода
Zn + 2HCl = $ZnCl_{2} + H_{2}$
2) с оксидами металлов
$CuO + H_{2}SO_{4}$ = $CuSO_{4} + H_{2}O$
$Fe_{2}O_{3} + 6HNO_{3}$ = $2Fe(NO_{3})_{3} + 3H_{2}O$
3) с гидроксидами металлов
$3Ca(OH)_{2} + 2H_{3}PO_{4}$ = $Ca_{3}(PO_{4})_{2} + 6H_{2}O$
$Al(OH)_{3} + 3HCl$ = $AlCl_{3} + 3H_{2}O$
4) с солями, если образуется ↑ или ↓
$CaCO_{3} + 2HNO_{3}$ = $Ca(NO_{3})_{2} + H_{2}O + CO_{2}$
$BaCl_{2} + H_{2}SO_{4}$ = $BaSO_{4} + 2HCl$
Задание №4
Бескислородные кислоты получают синтезом простых веществ:
$H_{2} + Cl_{2}$ = _
$H_{2} + S$ = _
Ответ:
Бескислородные кислоты получают синтезом простых веществ:
$H_{2} + Cl_{2}$ = 2HCl
$H_{2} + S$ = $H_{2}S$
Задание №5
Кислородсодержащие кислоты получают, если взаимодействуют:
1) кислотный оксид + $H_{2}O$ (тип реакции _ )
$N_{2}O_{3}$ + _ = _
$N_{2}O_{5}$ + _ = _
2) кислота + соль (тип реакции _ )
$HCl + AgNO_{3}$ = _ + _
$Ca_{3}(PO_{4})_{2} + H_{2}SO_{4}$ = _ + _
Ответ:
Кислородсодержащие кислоты получают, если взаимодействуют:
1) кислотный оксид + $H_{2}O$ (тип реакции соединение)
$N_{2}O_{3} + H_{2}O$ = $2HNO_{2}$
$N_{2}O_{5}$ + $H_{2}O$ = $2HNO_{3}$
2) кислота + соль (тип реакции обмена)
$HCl + AgNO_{3}$ = $AgCl + HNO_{3}$
$Ca_{3}(PO_{4})_{2} + 3H_{2}SO_{4}$ = $3CaSO_{4} + 2H_{3}PO_{4}$

