§28. Естественные семейства химических элементов. Амфотерность. Часть II
Задание №1
Выберите верное утверждение.
1) Классификация Берцелиуса верна, так как ее полностью подтверждает рассмотренные ранее генетические ряды металлов и неметаллов.
2) Классификация Берцелиуса относительна (не совсем верна).
Ответ: _
Аргументируйте свой ответ.
Ответ:
Ответ: 2
Й. Я. Берцелиус разделил все элементы на два класса − металлы и неметаллы на основе различий в свойствах образованных ими простых и сложных веществ. Так, металлам соответствуют основные оксиды и основания, а неметаллам − кислотные оксиды и кислоты. Так как классов было только два, они включали значительно отличающиеся друг от друга элементы. Наличие особых, двойственных свойств оксидов и гидроксидов у некоторых металлов противоречило предложенной Берцелиусом классификации.
Задание №2
Оформите схему.
Классификация солей
| - | - | - | - |
| Примеры | Примеры | Примеры | Примеры |
| 1) _ | 1) _ | 1) _ | 1) _ |
| 2) _ | 2) _ | 2) _ | 2) _ |
| 3) _ | 3) _ | 3) _ | 3) _ |
Ответ:
Классификация солей
| КОМПЛЕКСНЫЕ | КИСЛЫЕ | ОСНОВНЫЕ | СРЕДНИЕ, или НОРМАЛЬНЫЕ |
| Примеры | Примеры | Примеры | Примеры |
| 1) $K[Al(OH)_{4}]$ | 1) KHS | 1) Mg(OH)Cl | 1) $K_{2}SO_{4}$ |
| 2) $Na_{2}[Zn(OH)_{4}]$ | 2) $NaHSO_{4}$ | 2) $Zn(OH)NO_{3}$ | 2) NaCl |
| 3) $K_{2}[Zn(OH)_{4}]$ | 3) $K_{2}HPO_{4}$ | 3) $Ca(OH)NO_{3}$ | 3) $Li_{3}PO_{4}$ |
Задание №3
Выберите верное утверждение.
1) Для получения амфотерного гидроксида нужно по каплям приливать к раствору щелочи раствор соли.
2) Для получения амфотерного гидроксида нужно по каплям приливать к раствору соли раствор щелочи.
Ответ: _
Подтвердите ответ уравнениями реакций.
Ответ:
Ответ: 2
$3NaOH + AlCl_{3} = Al(OH)_{3} + 3NaCl$
При взаимодействии соли и избытка раствора щелочи образуется комплексная соль.
$AlCl_{3} + 4NaOH = Na[Al(OH)_{4}] + 3NaCl$
Задание №4
Напишите уравнения реакций следующих превращений: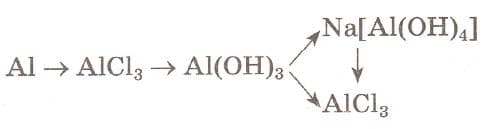
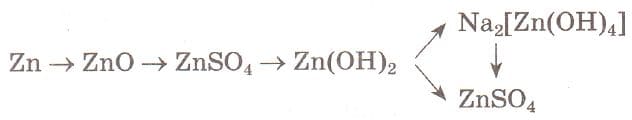
Ответ:
1.
$2Al + 3Cl_{2} = 2AlCl_{3}$
$AlCl_{3} + 3NaOH = 3NaCl + Al(OH)_{3}$
$Al(OH)_{3} + NaOH = Na[Al(OH)_{4}]$
$Al(OH)_{3} + 3HCl = AlCl_{3} + 3H_{2}O$
$Na[Al(OH)_{4} + 4HCl = NaCl + AlCl_{3} + 4H_{2}O$
2.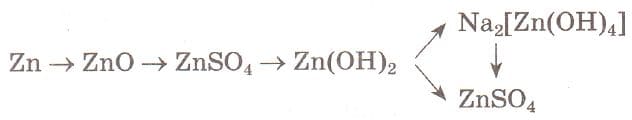
$2Zn + O_{2} = 2ZnO$
$ZnO + H_{2}SO_{4} = ZnSO_{4} + H_{2}O$
$ZnSO_{4} + 2NaOH = Na_{2}SO_{4} + Zn(OH)_{2}$
$Zn(OH)_{2} + 2NaOH = Na_{2}[Zn(OH)_{4}]$
$Zn(OH)_{2} + H_{2}SO_{4} = ZnSO_{4} + 2H_{2}O$
$Na_{2}[Zn(OH)_{4}] + 3H_{2}SO_{4} = 2NaHSO_{4} + ZnSO_{4} + 4H_{2}O$
Задание №5
Рассчитайте количество вещества гидроксида натрия, необходимого для перевода 483 г 10%−ного раствора сульфата цинка в сульфат натрия согласно уравнению
$ZnSO_{4} + 4NaOH = Na_{2}SO_{4} + Na_{2}ZnO_{2} + 2H_{2}O$
Рассчитайте количество выделившейся воды.
Ответ:
Дано:
$m_{р-ра}$ ($ZnSO_{4}$) = 483 г
ω = 10%
Найти:
n (NaOH) − ?
n ($H_{2}O$) − ?
Решение:
$ZnSO_{4} + 4NaOH = Na_{2}SO_{4} + Na_{2}ZnO_{2} + 2H_{2}O$
n (NaOH) = 4 * n ($ZnSO_{4}$)
n ($ZnSO_{4}$) = m : M
$m_{в-ва} (ZnSO_{4})$ = $m_{р-ра}$ ($ZnSO_{4}$) * ω
$m_{в-ва} (ZnSO_{4})$ = 483 г * 0,1 = 48,3 г
n ($ZnSO_{4}$) = 48,3 г : 161 г/моль = 0,3 моль
n (NaOH) = 4 * 0,3 моль = 1,2 моль
n ($H_{2}O$) = 0,5 * n (NaOH) = 0,5 * 1,2 моль = 0,6 моль
Ответ: n (NaOH) = 1,2 моль; n ($H_{2}O$) = 0,6 моль
Задание №6
Подготовьте 20 карточек для лабораторной работы к §29. На них напишите символы первых 20 химических элементов с указанием относительной атомной массы, характера простого вещества (металл или неметалл), формулы высших оксидов и гидроксидов (основания, кислородсодержащей кислоты или амфотерного гидроксида).
Ответ:
1) $^{1}_{1}H$ − неметалл
$H_{2}O$ − высший оксид и гидроксид
2) $^{4}_{2}He$ − благородный газ
Высший оксид − нет
Высший гидроксид − нет
3) $^{7}_{3}Li$ − металл
Высший оксид − $Li_{2}O$
Высший гидроксид − LiOH
4) $^{9}_{4}Be$ − металл
Высший оксид − BeO
Высший гидроксид − $Be(OH)_{2}$
5) $^{11}_{5}B$ − неметалл
Высший оксид − $B_{2}O_{3}$
Высший гидроксид − $H_{3}BO_{3}$
6) $^{12}_{6}C$ − неметалл
Высший оксид − $CO_{2}$
Высший гидроксид − $H_{2}CO_{3}$
7) $^{14}_{7}N$ − неметалл
Высший оксид − $N_{2}O_{5}$
Высший гидроксид − $HNO_{3}$
8) $^{16}_{8}O$ − неметалл
Высший оксид − нет
Высший гидроксид − нет
9) $^{19}_{9}F$ − неметалл
Высший оксид − $OF_{2}$
Высший гидроксид − нет
10) $^{20}_{10}Ne$ − благородный газ
Высший оксид − нет
Высший гидроксид − нет
11) $^{23}_{11}Na$ − металл
Высший оксид − $Na_{2}O$
Высший гидроксид − NaOH
12) $^{24}_{12}Mg$ − металл
Высший оксид − MgO
Высший гидроксид − $Mg(OH)_{2}$
13) $^{27}_{13}Al$ − металл
Высший оксид − $Al_{2}O_{3}$
Высший гидроксид − $Al(OH)_{3}$
14) $^{28}_{14}Si$ − неметалл
Высший оксид − $SiO_{2}$
Высший гидроксид − $H_{2}SiO_{3}$
15) $^{31}_{15}P$ − неметалл
Высший оксид − $P_{2}O_{5}$
Высший гидроксид − $H_{3}PO_{4}$
16) $^{32}_{16}S$ − неметалл
Высший оксид − $SO_{3}$
Высший гидроксид − $H_{2}SO_{4}$
17) $^{35,5}_{17}Cl$ − неметалл
Высший оксид − $Cl_{2}O_{7}$
Высший гидроксид − $HClO_{4}$
18) $^{40}_{18}Ar$ − благородный газ
Высший оксид − нет
Высший гидроксид − нет
19) $^{39}_{19}K$ − металл
Высший оксид − $K_{2}O$
Высший гидроксид − KOH
20) $^{40}_{20}Ca$ − металл
Высший оксид − CaO
Высший гидроксид − $Ca(OH)_{2}$

