Простые вещества - неметаллы. Часть 1
Задание №1
Неметаллы (НМ) располагаются в _ _ _ − _ _ _ группах. Только из НМ состоит _ _ _ _ группа, или группа _ _ _ _ _ _ _ _ _. По физическим свойствам к НМ следует отнести также _ _ _ _ _ группу, или группу _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _.
Ответ
Неметаллы (НМ) располагаются в III − VII группах. Только из НМ состоит VIIA группа, или группа галогенов. По физическим свойствам к НМ следует отнести также VIIA группу, или группу благородных газов.
Задание №2
У атомов неметаллов _ и более электрона во внешнем слое, небольшой радиус атома, например _ , у атома которого _ внешних e. Поэтому атомы НМ стремятся _ _ _ _ _ _ _ недостающие до 8e. Это свойство атомов характеризуется _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _. В соответствии с ним НМ образуют особый ряд:
_ _ _ _ _ _ _ _ _ _ _.
Ответ
У атомов неметаллов 4 и более электрона во внешнем слое, небольшой радиус атома, например $F_{2}$, у атома которого 7 внешних e. Поэтому атомы НМ стремятся принять недостающие до 8e. Это свойство атомов характеризуется электроотрицательностью. В соответствии с ним НМ образуют особый ряд:
H Si P Se C S Br Cl N O F.
Задание №3
Молекулы простых веществ НМ образованы за счет _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ связи. Двухатомные молекулы имеют, например, следующие простые вещества: _ $_{2}$, _ $_{2}$, _ $_{2}$, _ _ _ _ _ _ _ _; трехатомная молекула _ $_{3}$ − у _ _ _ _ _.
Ответ
Молекулы простых веществ НМ образованы за счет ковалентной неполярной связи. Двухатомные молекулы имеют, например, следующие простые вещества: $Cl_{2}$, $Br_{2}$, $F_{2}$, галогены; трехатомная молекула $O_{3}$ − у озона.
Задание №4
Аллотропия для неметаллов более характерна, чем для металлов.
Заполните таблицу "Аллотропные модификации неметаллов". Данные для таблицы найдите с помощью дополнительных источников информации, в том числе Интернета.
Ответ
Аллотропные модификации неметаллов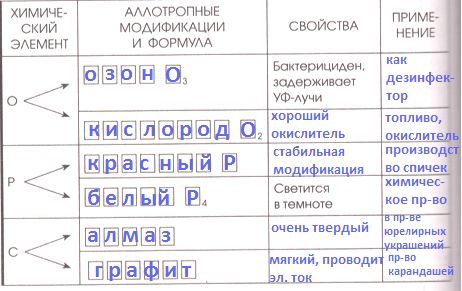
Задание №5
Заполните таблицу "Сравнение свойств металлов и неметаллов".
| Признаки сравнения | Металлы | Неметаллы | Примечания |
| Положение в Периодической системе | |||
| Особенности строения атомов: − число е во внешнем слое; − радиус атома | |||
| Химическая связь в простом веществе | |||
| Способность к аллотропии | |||
| Физические свойства: − блеск | + | - | Но у графита и йода металлический блеск. Но графит электропроводен. |
Ответ
Сравнение свойств металлов и неметаллов
| Признаки сравнения | Металлы | Неметаллы | Примечания |
| Положение в Периодической системе | I − III A группа, а также В подгруппы | III − VIIIA группы | |
| Особенности строения атомов: − число е во внешнем слое; − радиус атома | 1−3 е; большой радиус | 4−7 е; маленький радиус | |
| Химическая связь в простом веществе | Металлическая | Ковалентная неполярная | |
| Способность к аллотропии | Отсутствует | Характерна | |
| Физические свойства: − блеск | + | - | Но у графита и йода металлический блеск. Но графит электропроводен. |

