Оксиды и летучие водородные соединения. Часть 2
Задание №1
Поиграйте в "крестики−нолики". Покажите выигрышный путь, который составляют формулы высших оксидов элементов IV−VIA групп.
| $Na_{2}O$ | FeO | $N_{2}O_{5}$ |
| ZnO | $SO_{2}$ | $SO_{3}$ |
| $Al_{2}O_{3}$ | $P_{2}O_{5}$ | $CO_{2}$ |
Распределите все приведенные в таблице оксиды на две группы. Запишите их названия.
Оксиды металлов Оксиды неметаллов
Ответ
| $Na_{2}O$ | FeO | $N_{2}O_{5}$ |
| ZnO | $SO_{2}$ | $SO_{3}$ |
| $Al_{2}O_{3}$ | $P_{2}O_{5}$ | $CO_{2}$ |
$N_{2}O_{5}$, $SO_{3}$, $CO_{2}$ − выигрышный путь.
| Оксиды металлов | Оксиды неметаллов |
| $Na_{2}O$ − оксид натрия | $N_{2}O_{5}$ − оксид азота (V) |
| FeO − оксид железа (II) | $SO_{2}$ − оксид серы (IV) |
| ZnO − оксид цинка | $SO_{3}$ − оксид серы (VI) |
| $Al_{2}O_{3}$ − оксид алюминия | $P_{2}O_{5}$ − оксид фосфора (V) |
| $CO_{2}$ − оксид углерода (IV) |
Задание №2
Впишите в соответствующие столбцы формулы следующих соединений: $P_{2}O_{3}, BaH_{2}, NO, SiH_{4}, H_{2}S, H_{2}O_{2}, KH, Cr_{2}O_{3}, HBr, AlH_{3}, OF_{2}$.
Укажите их названия.
Оксиды Гидриды Летучие водородные соединения
Ответ
| Оксиды | Гидриды | Летучие водородные соединения |
| $P_{2}O_{3}$ − оксид фосфора (III) | $BaH_{2}$ − гидрид бария | $SiH_{4}$ − силан |
| NO − оксид азота (II) | KH − гидрид калия | $H_{2}S$ − сероводород |
| $Cr_{2}O_{3}$ − оксид хрома (III) | $AlH_{3}$ − гидрид алюминия | HBr − бромоводород |
Задание №3
Поиграйте в "крестики−нолики". Покажите выигрышный путь, который составляют формулы гидридов.
| KH | $H_{2}O$ | CO |
| $BaH_{2}$ | CuO | NaOH |
| $CaH_{2}$ | $NH_{3}$ | $Li_{2}O$ |
Ответ
| KH | $H_{2}O$ | CO |
| $BaH_{2}$ | CuO | NaOH |
| $CaH_{2}$ | $NH_{3}$ | $Li_{2}O$ |
Гидриды: $KH, BaH_{2}, CaH_{2}$.
Задание №4
Напишите формулы оксидов и летучих водородных соединений следующих химических элементов:
1) углерода (IV)
2) азота (III)
3) серы (VI)
Ответ
1) $CO_{2}, CH_{4}$
2) $N_{2}O_{3}, NH_{3}$
3) $SO_{3}, H_{2}S$
Задание №5
Дополните таблицу.
| Название оксида | Формула | Нахождение в природе |
| Оксид водорода | ||
| $CO_{2}$ | ||
| $Al_{2}O_{3}, SiO_{2}$ |
Ответ
| Название оксида | Формула | Нахождение в природе |
| Оксид водорода | $H_{2}O$ | Гидросфера |
| Оксид углерода (IV) | $CO_{2}$ | Атмосфера |
| Оксид алюминия и оксид кремния | $Al_{2}O_{3}, SiO_{2}$ | Глина |
Задание №6
Назовите оксиды азота и рассчитайте массовую долю азота в них.
1) $Na_{2}O$ _ ω(N) = _
2) NO _ ω(N) = _
3) $N_{2}O_{3}$ _ ω(N) = _
4) $NO_{2}$ _ ω(N) = _
5) $N_{2}O_{5}$ _ ω(N) = _
Сделайте вывод: с увеличением с.о. азота в оксиде массовая доля данного химического элемента _ _ _ _ _ _ _ _ _ _ _ . Постройте схематический график данной зависимости.

Ответ
1) $Na_{2}O$ − оксид натрия
ω(N) = 64%
2) NO − оксид азота (II)
ω(N) = 47%
3) $N_{2}O_{3}$ − оксид азота (III)
ω(N) = 37%
4) $NO_{2}$ − оксид азота (IV)
ω(N) = 30%
5) $N_{2}O_{5}$ − оксид азота (V)
ω(N) = 26%
Сделайте вывод: с увеличением с.о. азота в оксиде массовая доля данного химического элемента уменьшается.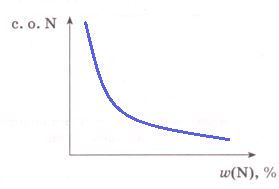
Задание №7
Сколько $м^{3}$ содержится в 45,75 кг оксида хлора (VII)?
Ответ
Дано:
m ($Cl_{2}O_{7}$) = 45,75 кг
Найти:
V ($Cl_{2}O_{7}$) − ?
Решение:
V ($Cl_{2}O_{7}$) = n * $V_{m}$ = m : M * $V_{m}$
M ($Cl_{2}O_{7}$) = 35,5 * 2 + 16 * 7 = 183 г/моль
V ($Cl_{2}O_{7}$) = 45,75 кг : 183 г/моль * 22,4 л/моль = 5,6 $м^{3}$
Ответ: V ($Cl_{2}O_{7}$) = 5,6 $м^{3}$
Задание №8
Найдите количество вещества атомов кислорода и атомов фосфора, которое содержится в оксиде фосфора (III) массой 220 г.
Решение:
1) n ( _ ) = _
2) Анализформулы оксида фосфора (III) показывает, что n (P) = 2 * n ( _ ), а n (O) = 3 * n ( _ )
3) N (P) = _
4) N (O) = _
Ответ: _
Ответ
Дано:
m ($P_{2}O_{3}$) = 220 г
Найти:
n (O) − ?
n (P) − ?
Решение:
1) n ($P_{2}O_{3}$) = m : M
M ($P_{2}O_{3}$) = 31 * 2 + 16 * 3 = 110 г/моль
n ($P_{2}O_{3}$) = 220 г : 110 г/моль = 2 моль
2) Анализформулы оксида фосфора (III) показывает, что n (P) = 2 * n ($P_{2}O_{3}$), а n (O) = 3 * n ($P_{2}O_{3}$)
3) N (P) = n (P) * Na = 2 * 2 моль * $6 * 10^{23}$ молекул/моль = $24 * 10^{23}$ молекул
N (O) = n (O) * Na = 3 * 2 моль * $6 * 10^{23}$ молекул/моль = $36 * 10^{23}$ молекул
Ответ: N (P) = $24 * 10^{23}$ молекул; N (O) = $36 * 10^{23}$ молекул

