Основания, их классификация и химические свойства в свете ТЭД. Часть 1
Задание №1
Основания − это _
Ответ
Основания − это сложные вещества, состоящие из катиона металла и гидроксогрупп.
Задание №2
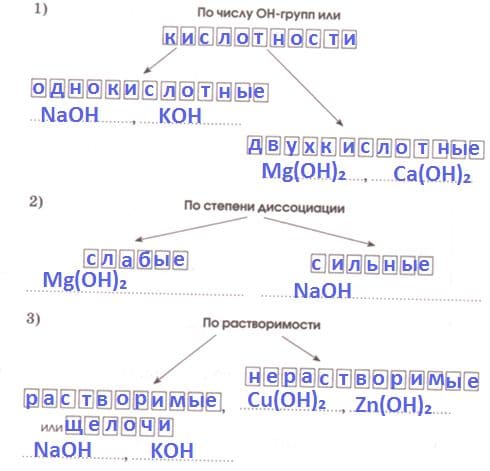
Вспомните классификацию оснований и распределите гидроксид натрия, гидроксид магния, гидроксид кальция, гидроксид аммиака по соответствующим группам, вписав их формулы.
Ответ
Задание №3
Общие химические свойства оснований.
| ЩЁЛОЧИ | НЕРАСТВОРИМЫЕ ОСНОВАНИЯ |
| 1) Щёлочь + _ _ _ _ _ _ _ → _ _ _ _ + _ _ _ _ (реакция _ _ _ _ _ _ _ _ _ _ _ _ _ ) | 1) Нерастворимое основание + _ _ _ _ _ _ _ → _ _ _ _ + _ _ _ _ |
| 2) Щёлочь + _ _ _ _ _ _ _ _ _ _ _ _ _ _ → _ _ _ _ + _ _ _ _ |
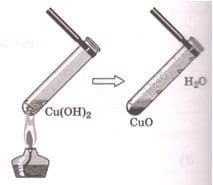
2) Разлагается при нагревании: нерастворимое основание → _ _ _ _ _ _ _ _ _ _ _ _ + _ _ _ _
|
| 3) Щёлочь + _ _ _ _ → новая _ _ _ _ + новое _ _ _ _ _ _ _ _ _, если выделяется газ ↑ или выпадает осадок ↓ |
Ответ
Общие химические свойства оснований.
| ЩЁЛОЧИ | НЕРАСТВОРИМЫЕ ОСНОВАНИЯ |
| 1) Щёлочь + кислота → соль + вода (реакция нейтрализации | 1) Нерастворимое основание + кислота → соль + вода |
| 2) Щёлочь + оксид неметалла → соль + вода |
2) Разлагается при нагревании: нерастворимое основание → оксид металла + вода
|
| 3) Щёлочь + соль → новая соль + новое основание, если выделяется газ ↑ или выпадает осадок ↓ |
Задание №4
Приведите примеры уравнений реакций, характеризующих общие свойства оснований, в молекулярном, полном ионном и сокращенном ионном видах.
1) $H_{2}SO_{4} + ...NaOH → ... + ... $
2) $H_{2}SO_{4} + ...Cu(OH)_{2} → ... + ... $
3) $SO_{3} + ... → Na_{2}SO_{4} + ...$
4) $...Fe(OH)_{3} → ... + ...$
5) $...KOH + ... → Cu(OH)_{2}↓ + ...$
6) $Ba(OH)_{2} + ... → BaSO_{4}↓ + NaOH$
7) $NH_{4}Cl + ... → NaCl + NH_{3} + H_{2}O$
Ответ
1) $H_{2}SO_{4} + 2NaOH → Na_{2}SO_{4} + 2H_{2}O$
$2H^{+} + SO_{4}^{2-} + 2Na^{+} + 2OH^{-} → 2Na^{+} + SO_{4}^{2-} + 2H_{2}O$
$2H^{+} + 2OH^{-} → 2H_{2}O$
2) $H_{2}SO_{4} + Cu(OH)_{2} → CuSO_{4} + 2H_{2}O$
$2H^{+} + SO_{4}^{2-} + Cu(OH)_{2} → Cu^{2+} + SO_{4}^{2-} + 2H_{2}O$
$2H^{+} + Cu(OH)_{2} → Cu^{2+} + 2H_{2}O$
3) $SO_{3} + 2NaOH → Na_{2}SO_{4} + H_{2}O$
$SO_{3} + 2Na^{+} + 2OH^{-} → 2Na^{+} + SO^{2-}_{4} + H_{2}O$
$SO_{3} + 2OH^{-} → SO^{2-}_{4} + H_{2}O$
4) $2Fe(OH)_{3} → Fe_{2}O_{3} + 3H_{2}O$
$2Fe(OH)_{3} → Fe_{2}O_{3} + 3H_{2}O$
$2Fe(OH)_{3} → Fe_{2}O_{3} + 3H_{2}O$
Ионное уравнение совпадает с молекулярным!
5) $2KOH + CuCl_{2} → Cu(OH)_{2}↓ + 2KCl$
$2K^{+} + 2OH^{-} + Cu^{2+} + 2Cl^{-} → Cu(OH)_{2}↓ + 2K^{+} + 2Cl^{-}$
$2OH^{-} + Cu^{2+} → Cu(OH)_{2}↓$
6) $Ba(OH)_{2} + Na_{2}SO_{4} → BaSO_{4}↓ + 2NaOH$
$2Ba^{2+} + 2OH^{-} + 2Na^{+} + SO_{4}^{2-} → BaSO_{4}↓ + 2Na^{+} + 2OH^{-}$
$2Ba^{2+} + SO_{4}^{2-} → BaSO_{4}↓$
7) $NH_{4}Cl + NaOH → NaCl + NH_{3} + H_{2}O$
$NH_{4}^{+} + Cl^{-} + Na^{+} + OH^{-} → Na^{+} + Cl^{-} + NH_{3} + H_{2}O$
$NH_{4}^{+} + OH^{-} → NH_{3} + H_{2}O$